Verschil tussen peptiden en peptonen
 Share
Share
De grootste verschil tussen peptiden en peptonen is dat peptiden zijn korte ketens van aminozuren gekoppeld door peptidebindingen, terwijl peptonen een klasse van peptiden zijn, het resultaat van de proteolyse van dierlijke melk of vlees. Peptiden zijn een mengsel van dipeptiden, tripeptiden, tetrapeptide, enz. Peptonen bevatten echter vetten, zouten, metalen, vitaminen, enz. Bovendien dienen peptiden als hormonen, neuropeptiden, alkaloïden, antibiotica en structurele moleculen. Maar peptonen dienen als een bron van stikstof en koolstof.
Peptiden en peptonen zijn twee soorten moleculen die naar voren komen als gevolg van de hydrolyse van eiwitten. Beide zijn opgebouwd uit aminozuren. De basiselementen van beide zijn koolstof, zuurstof, waterstof, stikstof en zwavel.
Key Areas Covered
1. Wat zijn peptiden
- Definitie, structuur, belang
2. Wat zijn Peptones
- Definitie, structuur, belang
3. Wat zijn de overeenkomsten tussen peptiden en peptonen
- Overzicht van gemeenschappelijke functies
4. Wat is het verschil tussen peptiden en peptonen
- Vergelijking van belangrijke verschillen
Sleutelbegrippen: aminozuren, peptidenbanden, peptiden, peptonen, proteïnen

Wat zijn peptiden
Peptiden zijn verbindingen met twee of meer aminozuren verbonden in een keten; de carboxylgroep van elk zuur is verbonden met de aminogroep van de volgende door een binding van het type -OC-NH-. Dit bindingstype wordt peptidebindingen genoemd. In feite zijn eiwitten polypeptiden. De vijf klassen van peptiden zijn melkpeptiden, ribosomale peptiden, niet-ribosomale peptiden, peptonen en peptidefragmenten..
- Melkpeptiden - Gevormd uit melkeiwit, caseïne.
- Ribosomale peptiden - gevormd uit de proteolytische digestie van polypeptiden gesynthetiseerd tijdens de translatie van mRNA
- Niet-ribosomale eiwitten - Geassembleerd door de enzymen, maar niet door de translatie van mRNA (bijv. Glutathione)
- Peptones - Gevormd door de proteolytische vertering van dierlijke melk of vlees
- Peptidefragmenten - Eiwitfragmenten die worden gebruikt voor de identificatie of kwantificatie van de eiwitbron
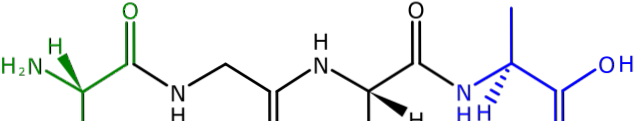
Figuur 1: Tetrapeptide
Peptiden zijn functionele moleculen in het lichaam die dienen als hormonen, neuropeptiden, alkaloïden en antibiotica. Ze dienen ook als structurele moleculen in de cel.
Wat zijn Peptones
Peptonen verwijzen naar de oplosbare eiwitten gevormd in het vroege stadium van eiwitafbraak tijdens de spijsvertering. De spijsverteringsenzymen van het maag- en pancreassap zijn verantwoordelijk voor de afbraak van eiwitten in peptonen. Peptonen worden chemisch gesynthetiseerd door een eiwitbron te koken met water en verdunde zuren. De drie soorten pure peptonen zijn amfopeptone, antipeptone en hemipeptone.

Figuur 2: Agarplaat met trypton
Peptonen zijn een ingrediënt van de voedingsmedia die worden gebruikt voor bacteriën en schimmels. Trypton is een dergelijk pepton dat gewoonlijk wordt gebruikt in de moleculaire biologie. Het wordt gevormd door de vertering van caseïne.
Overeenkomsten tussen peptiden en peptonen
- Peptiden en peptonen zijn twee soorten eiwitten gemaakt van aminozuren.
- De elementen van peptiden en peptonen zijn koolstof, waterstof, zuurstof, stikstof en zwavel.
- Beide zijn afbraakproducten van de hydrolyse van eiwitten.
- Ze precipiteren niet met ammoniumzwavel.
Verschil tussen peptiden en peptonen
Definitie
peptiden: Verbindingen met twee of meer aminozuren verbonden in een keten, waarbij de carboxylgroep van elk zuur is verbonden met de aminogroep van de volgende door een binding van het type -OC-NH-
peptonen: Oplosbare eiwitten gevormd in het vroege stadium van eiwitafbraak tijdens de spijsvertering.
Betekenis
peptiden: Korte ketens van aminozuren
peptonen: Een klasse van peptiden
Afgeleid van
peptiden: Er zijn verschillende klassen van peptiden gebaseerd op de manier waarop ze worden geproduceerd
peptonen: Proteolyse van dierlijke melk of vlees
Samenstelling
peptiden: Dipeptiden, tripeptiden, tetrapeptiden, enz.
peptonen: Naast kleine peptiden bevatten vetten, zouten, metalen, vitamines, enz.
Types
peptiden: De vijf klassen van peptiden zijn melkpeptiden, ribosomale peptiden, niet-ribosomale peptiden, peptonen en peptidefragmenten.
peptonen: De drie soorten pure peptonen zijn amfopeptone, antipeptone en hemipeptone
Belang
peptiden: Dienen als hormonen, neuropeptiden, alkaloïden, antibiotica en structurele moleculen
peptonen: Gebruikt in voedingsmedia voor de groei van bacteriën en schimmels
Conclusie
Peptiden zijn korte ketens van aminozuren, terwijl peptonen een klasse van peptiden zijn die worden gevormd door de proteolyse van dierlijke melk of vlees. Zowel peptiden als peptonen zijn de resultaten van de hydrolyse van eiwitten. Het belangrijkste verschil tussen peptiden en peptonen is de vorming en de samenstelling.
Referentie:
1. "Peptide." Nature News, Nature Publishing Group, hier beschikbaar
2. "Peptone." Fine Dictionary, hier beschikbaar
Afbeelding met dank aan:
1. "Tetrapeptide structurele formules" door Ipatrol - Eigen werk (CC0) via Commons Wikimedia
2. "Rhizobium tropici stam BR816 op TY agar" door Ninjatacoshell - Eigen werk (CC BY-SA 3.0) via Commons Wikimedia

