Verschil tussen verestering en transverestering
 Share
Share
Belangrijkste verschil - Esterificatie versus transverestering
Verestering en transverestering zijn twee termen die verband houden met esters. Esters zijn chemische verbindingen die zijn afgeleid van een zuur door de -OH-groep te vervangen door een alkoxygroep. Esters worden typisch gevormd uit carbonzuren. Het zijn polaire moleculen en kunnen waterstofbruggen vormen met andere moleculen door de aanwezigheid van zuurstofatomen. Verestering is het proces dat wordt gebruikt om een ester te produceren. Transverestering is de modificatie van esters door chemische reacties. Het belangrijkste verschil tussen verestering en transverestering is dat verestering omvat een ester als het eindproduct terwijl transverestering een ester als een reactant omvat.
Key Areas Covered
1. Wat is verestering
- Definitie, mechanisme, voorbeelden
2. Wat is transverestering
- Definitie, mechanisme, voorbeelden
3. Wat is het verschil tussen verestering en transverestering
- Vergelijking van belangrijke verschillen
Sleutelbegrippen: alcohol, alkoxygroep, carboxylzuren, verestering, esters, transverestering
Wat is verestering
Verestering is het proces waarbij een ester wordt gevormd. Meestal gebeurt dit met carbonzuren. Verestering treedt op wanneer een carbonzuur reageert met een alcohol. Deze reactie is alleen mogelijk wanneer een zure katalysator en warmte aan het reactiemengsel worden verschaft. Anders zal er geen reactie zijn, zelfs als het carbonzuur en de alcohol met elkaar worden gemengd. Dit komt omdat dit proces een hoge energie nodig heeft om de -OH-groep uit het carbonzuur te verwijderen. Daarom is een katalysator nodig om de activeringsenergie van de reactie te verminderen en is warmte als een energiebron vereist.
Het bijproduct gevormd in deze reactie is water. Daarom kunnen we in aanwezigheid van een dehydratatiemiddel het zuivere esterproduct verkrijgen. Door het carbonzuur of de alcohol te veranderen, kan de ester met gewenste koolstofatomen worden verkregen. De veresteringsreactie is een evenwichtsreactie. Daarom, om een hoge opbrengst aan ester te verkrijgen, kunnen we ofwel een overmatige hoeveelheid alcohol of een dehydratatiemiddel gebruiken om water uit het systeem te verwijderen. Als dat niet het geval is, kan water worden verwijderd met een andere methode, zoals destillatie.

Figuur 01: Synthese van methylacetaat
De bovenstaande afbeelding toont de productie van methylacetaat met behulp van ethaanzuur en methanol als reagentia. Het bijproduct is een watermolecuul. Het watermolecuul wordt gevormd uit de H+ komt van alcohol en de -OH van het carbonzuur. De hier toegepaste katalysator is zwavelzuur.
Wat is transverestering
Transverestering is de uitwisseling van de alkylgroep bevestigd aan het zuurstofatoom van de ester met de alkylgroep van een alcohol. Deze reactie vereist zure of basische katalysatoren om de activeringsenergie van de reactie te verminderen.
Mechanisme
Transesterificatie van een ester wordt geïnitieerd met de nucleofiele aanval door de alcohol. De alcohol, die het proton verwijdert dat aan het zuurstofatoom is bevestigd, wordt een nucleofiel vanwege de aanwezigheid van elektronenparen. Deze nucleofiel kan het koolstofatoom aanvallen dat aan de twee zuurstofatomen is gehecht. Het koolstofatoom krijgt een gedeeltelijke positieve lading omdat de twee zuurstofatomen de bindingselektronen naar zich toe trekken, omdat de elektronenaffiniteit van de zuurstofatomen hoger is dan die van het koolstofatoom. Dus deze koolstof met de gedeeltelijke positieve lading is een goede locatie voor de nucleofiel om aan te vallen.
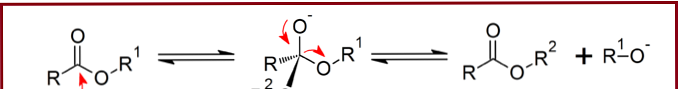
- Figuur 02: Transveresteringsreactie
Dit vormt een tussenmolecuul dat is samengesteld uit ester en alcohol gebonden aan het koolstofatoom (met gedeeltelijke positieve lading) door zijn zuurstof. Aangezien dit tussenproduct onstabiel is, vindt een herschikking plaats. Daar wordt de -OR-groep van carbonzuur verwijderd. Maar de alcoholgroep blijft gehecht aan de koolstof. Nu wordt een nieuwe ester gevormd.
Dit mechanisme wordt gebruikt bij de productie van polyester.
Verschil tussen verestering en transverestering
Definitie
verestering: Verestering is het proces waarbij een ester wordt gevormd.
omesteringstijd: Transverestering is de uitwisseling van de alkylgroep bevestigd aan het zuurstofatoom van de ester met de alkylgroep van een alcohol.
ester
verestering: De ester is het eindproduct van verestering.
omesteringstijd: De ester is een reactant van de transverestering.
bijproduct
verestering: Het bijproduct van verestering is een watermolecuul.
omesteringstijd: Het bijproduct van transverestering is een nucleofiel / een alcoholmolecuul.
Catalyst
verestering: Verestering vereist een zure katalysator.
omesteringstijd: Omestering vereist zure of basische katalysatoren of enzymen.
Energiebehoefte
verestering: Verestering vereist warmte-energie om de ester te produceren.
omesteringstijd: Transverestering vereist geen warmte.
Conclusie
Verestering is het proces waarbij een ester wordt gevormd. Transverestering is het proces waarbij een ester wordt gemodificeerd. De ester geproduceerd uit de verestering kan worden veranderd van transverestering om de gewenste ester te verkrijgen. Het belangrijkste verschil tussen verestering en transverestering is dat verestering een ester als het eindproduct omvat, terwijl transverestering een ester als reactant omvat.
Referenties:
1. "Verestering: definitie, proces en reacties." Study.com. Study.com, n.d. Web. Beschikbaar Hier. 4 aug. 2017.
2. "Transverestering." Wikipedia. Wikimedia Foundation, 1 augustus 2017. Web. Beschikbaar Hier. 4 aug. 2017.
Afbeelding met dank aan:
1. "Verestering (azijnzuur en methanol)" door Doxepine - Eigen werk, Public Domain) via Commons Wikimedia
2. "Algemeen transveresteringsmechanisme" door Rifleman 82 - Eigen werk, publiek domein) via Commons Wikimedia

